[本站讯]近日,药学院沈月毛/李瑶瑶教授团队的研究成果“Discovery and Biosynthesis of Pseudoamides Reveal Enzymatic Cyclization of the Polyene Precursor to 5–5 Bicyclic Tetramate Macrolactams”在ACS Catalysis上在线发表。药学院李瑶瑶教授为论文通讯作者,博士研究生李雪和硕士研究生刘清清为论文共同第一作者,山东大学药学院为第一完成单位和通讯作者单位。山东大学药学院教授沈月毛、微生物技术研究院副教授王浩鑫,内布拉斯加州立大学教授杜良成参与该项研究。
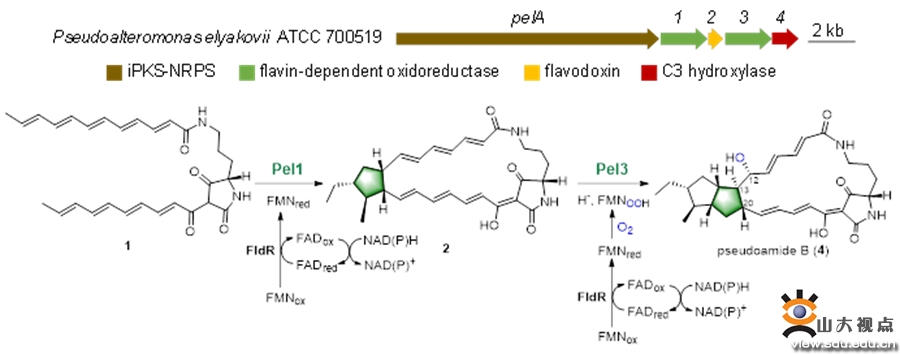
Polycyclic tetramate macrolactam (PoTeM)是一类含有特特拉姆酸结构单元及多环体系的大环内酰胺类化合物,以其新颖的化学结构、显著的生理活性和独特的作用机理正逐渐形成一个新的抗生素家族,具有良好开发应用前景。目前,尽管报道了多个PoTeMs的生物合成途径,但是其5-5双环合成相关的新颖酶学机制仍处于假说阶段。
针对上述问题,该研究以从交替假单胞菌(Pseudoalteromonas elyakovii) ATCC 700519中定向发现的新5-5双环PoTeM类化合物pseudoamides为研究对象。通过体内基因缺失、体外生化和同位素标记实验,阐明了pseudoamides中5-5双环合成机制。研究显示,黄素依赖性氧化还原酶Pel1和Pel3负责5-5双环合成,且其催化功能依赖还原伴侣进行电子传递。其中,Pel1通过还原性[2+3]环加成反应合成外侧5元环,引入的两个氢分别来自FMNH2和H2O;Pel3通过FMN-C4a-hydroxyperoxide实现C13-C20环化与C12羟基化偶联反应,合成内侧5元环,C12羟基氧来源于O2。上述研究为PoTeMs多环体系合成机制的深入解析和全新环系改造奠定了基础。
该研究得到了国家自然科学基金面上的项目资助。
文章链接:https://pubs.acs.org/doi/10.1021/acscatal.2c05784