[本站讯]11月16日,基础医学院教授马春红、副教授李春阳和药学院教授刘新泳作为共同通讯作者在Science Translational Medicine上发表了题为“Identification of a small-molecule Tim-3 inhibitor to potentiate T cell-mediated antitumor immunotherapy in preclinical mouse models”的研究论文。基础医学院博士研究生马帅雅、博士后田野和硕士毕业生彭加丽为本文的共同第一作者。山东大学为文章第一作者和通讯作者单位。
以PD-1/PD-L1为靶点的免疫检查点阻断疗法(Immune checkpoint blockade, ICB)在多种恶性肿瘤临床治疗中取得了显著的治疗效果。然而,该疗法仍面临临床响应率低和继发治疗抵抗的问题。因此,寻找新的免疫治疗靶点并开发其抑制剂,对于提高免疫治疗效果具有重要意义。其中,Tim-3是众多新兴免疫检查点分子中最有前景的靶点之一。马春红团队长期关注Tim-3,前期的系列研究揭示感染和炎症促进Tim-3表达,调控多种免疫细胞尤其是NK细胞和CD8+T细胞功能,导致免疫耗竭,进而加速炎癌转化;阐明了Tim-3与其配体磷脂酰丝氨酸(PtdSer)结合介导免疫细胞功能耗竭的分子机制,并在肝癌组织中表征了Tim-3介导的细胞空间互作网络。
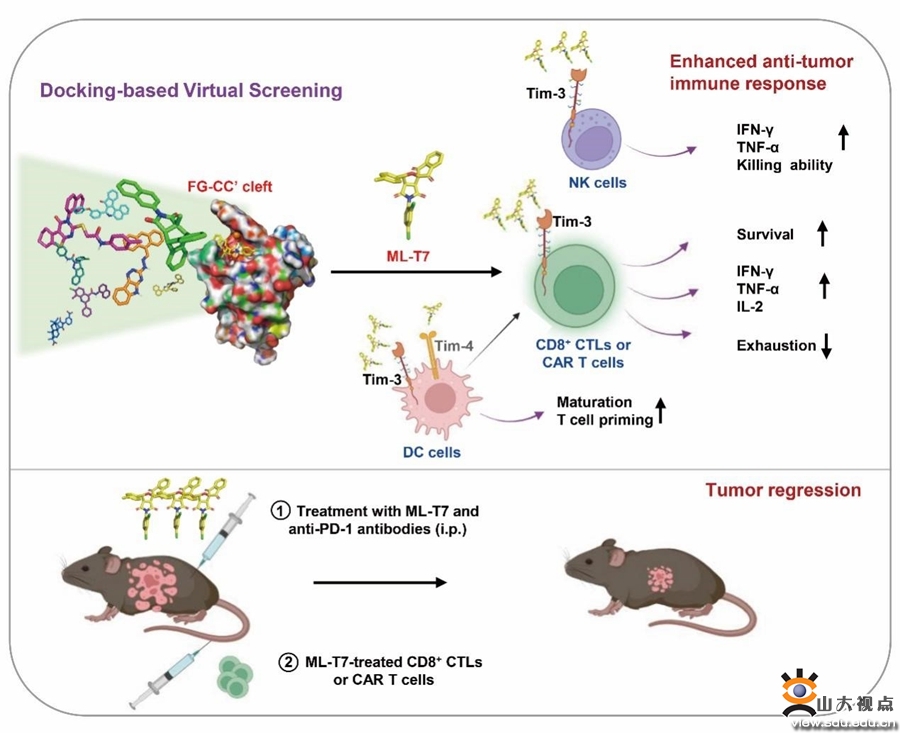
该文章利用虚拟筛选结合功能筛选的方法,鉴定到了一种Tim-3小分子抑制剂(命名为ML-T7);发现其不仅可以增强小鼠CD8+T细胞和人CAR T细胞的回输治疗效果,而且可以促进NK细胞杀伤肿瘤能力和DC细胞的抗原呈递能力;该化合物在多种肿瘤模型中可以发挥直接的抗肿瘤治疗效果,并增强PD-1抗体的免疫治疗效果。总之,文章报道了一项靶向Tim-3小分子化合物的系统筛选工作,证明了FG-CC'环结构在Tim-3抑制剂筛选中的重要意义,为开发靶向Tim-3的药物开发提供了新思路和理论基础。同时,鉴定出的ML-T7在临床前小鼠肿瘤模型中表现出较好的抗肿瘤活性,对其进一步优化改造具有重要的临床转化意义。
该工作得到中国科学院分子细胞卓越中心研究员王红艳提供的诸多帮助和材料支持、山东大学基础医学院研究员魏健提供的建议和帮助,以及山东大学转化医学共享平台的支持。该研究得到国家重点研发计划、国家自然科学基金、山东省泰山学者攀登计划、中国科协青年人才托举工程、中国博士后创新人才计划和山东大学青年学者未来计划等项目的资助。
马春红教授团队长期致力于肝脏免疫微环境调控和干预策略研究,系统探索HBV、代谢等环境因素诱发肝脏炎症及其恶性转化机制,为肿瘤免疫治疗提供了潜在靶点和新思路。相关成果相继发表在J Exp Med,Gastroenterology,Gut,J Hepatol,Nat Commun,Hepatology,Adv Sci,Cancer Res,Cell Death Differ,Mol Ther,Cell Mol Immunol,Signal Transduct Target Ther,Cell Reports,J Am Chem Soc等国际主流学术期刊。
刘新泳教授团队长期致力基于靶标结构和多种药物化学策略相结合的药物研究工作,聚焦于抗病毒药物、重大慢性病药物和免疫调节剂的先导发现、优化和药物开发。近年来已有多个抗病毒、抗痛风创新药物实现成果转化,相关成果在J Med Chem等权威期刊累计发表SCI论文400余篇。
原文链接:https://www.science.org/doi/10.1126/scitranslmed.adg6752