[本站讯]近日,微生物技术国家重点实验室高翔教授团队在肠道脆弱拟杆菌分泌的泛素同源蛋白BfUbb调节人肠道中菌间拮抗方面取得重要进展,相关研究成果以“Bacteroides fragilisubiquitin homologue drives intraspecies bacterial competition in the gut microbiome”为题发表在微生物领域Top期刊Nature Microbiology (中科院1区)。山东大学副研究员姜昆,博士研究生李伟勋、童明,博士后徐京华,博士研究生陈喆为论文共同第一作者,山东大学教授高翔为该论文唯一通讯作者,山东大学为第一完成单位和通讯作者单位。
人类肠道中有着极其密集和多样化的微生物群落。这个复杂的生态系统主要由不同种类的细菌组成,它们在有限的肠道内争夺资源和生态位,对人体健康具有极其重要的影响。拟杆菌是人体肠道中丰度最高的革兰氏阴性菌。为了在菌间竞争中获取优势地位,研究显示肠道拟杆菌开发了多种特定的杀菌蛋白作为对抗其他拟杆菌的抗菌武器。泛素分子长期以来被认为是真核细胞所特有的,但研究人员在前期的研究中却意外地发现人肠道脆弱拟杆菌(Bacteroides fragilis)可以编码并分泌一种具有杀菌活性的泛素同源蛋白(BfUbb),但其具体的杀菌机制及生理意义不为人知。
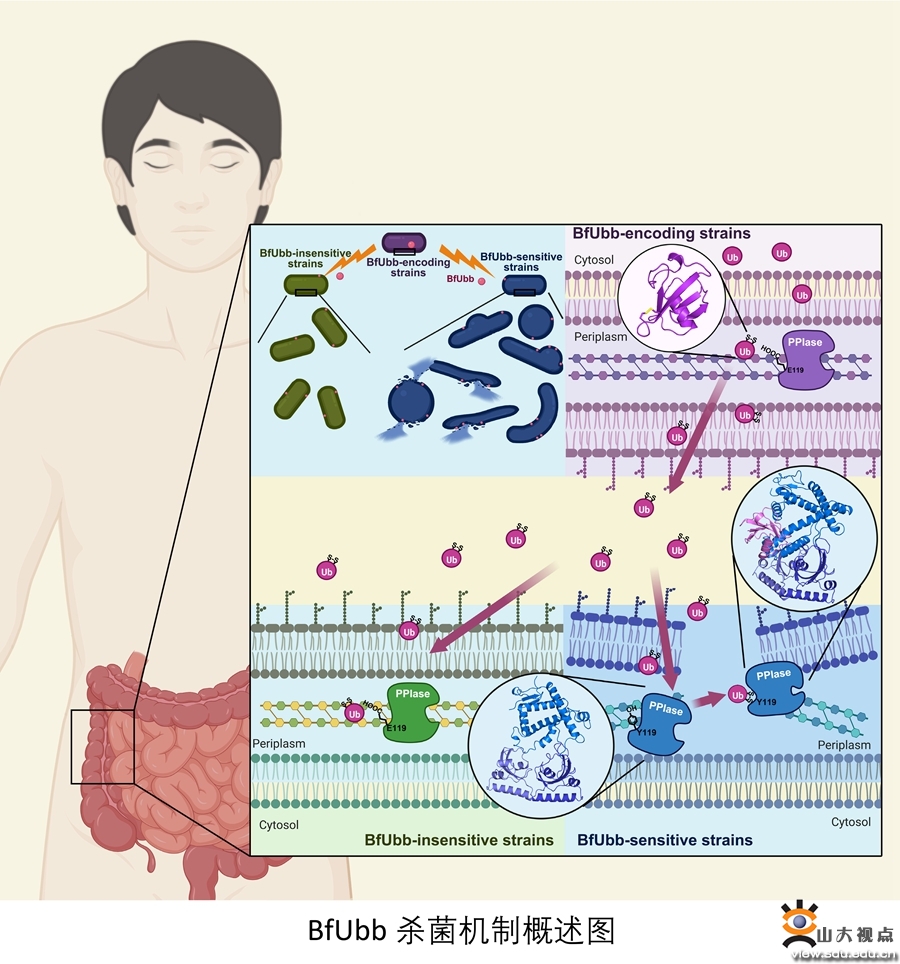
在该研究中,作者证明纯化的BfUbb蛋白的杀菌活性甚至比实验中用来抑制拟杆菌生长的四环素和氯霉素等抗生素的最小抑菌浓度还要低100倍以上。借助激光共聚焦显微镜,研究人员首次揭示了BfUbb在敏感菌株的周质空间中发挥毒性的杀菌表型。通过亲和共纯化串联质谱分析并结合相应的功能研究,作者证明BfUbb通过靶向拟杆菌周质空间中一个关键的脯氨酸顺反异构酶(PPIase)发挥杀菌活性。通过生物信息学分析,BfUbb-PPIase的复合物结构解析和分析,以及一系列的功能验证,作者惊讶地发现BfUbb通过其C末端二硫键介导与PPIase中119位酪氨酸(Tyr119)的相互作用决定了PPIase与BfUbb的结合特异性及菌株对BfUbb的敏感性。非敏感型脆弱拟杆菌中PPIase上119位氨基酸为谷氨酸(Glu119),从而逃避了BfUbb的结合,并获得了对BfUbb的抗性。同时,为了验证BfUbb的生理学意义,研究人员通过菌株水平的共培养实验、小鼠水平的共定殖实验及人体肠道菌群宏基因组数据分析证明BfUbb可使其生产菌株相对于其敏感菌株在人类肠道中获得巨大的竞争优势。
该研究系统深入地揭示了一种前所未有的肠道拟杆菌分泌的泛素同源蛋白拮抗特定肠道拟杆菌的杀菌机制,并表明BfUbb是塑造人类肠道内菌株组成的强大驱动因子,具有重要的应用潜力。该研究工作得到了国家自然科学基金、国家重点研发计划、山东省自然科学基金等基金的资助。山东大学微生物技术国家重点实验室生命环境研究公共技术平台为本工作提供了重要技术支持。
原文链接:https://www.nature.com/articles/s41564-023-01541-5