[本站讯]近日,国家自然科学基金委员会发布通知,齐鲁医院络病理论创新转化全国重点实验室张运院士作为项目负责人申请的国家自然科学基金重点项目《脂肪细胞钠尿肽受体C在脂质代谢和动脉粥样硬化中的作用机制和转化研究》和张铭湘教授作为项目负责人申请的国家自然科学基金重点项目《ILF3介导糖基化终末产物代谢失衡加速糖尿病血管钙化分子机制研究》获批立项。此外,张文程教授、王双喜教授、张杰副教授各获批1项国家自然科学基金面上项目,宋铭主治医师、刘晓琳医师、博士后薛飞和博士后俞力雯各获得1项国家自然科学基金青年项目。在基础研究领域中,张铭湘教授团队和王双喜教授团队取得系列重要进展,在Nature子刊Nature Communications (中科院一区,最新影响因子14.7)发表系列论文,受到国际学术界的高度关注。
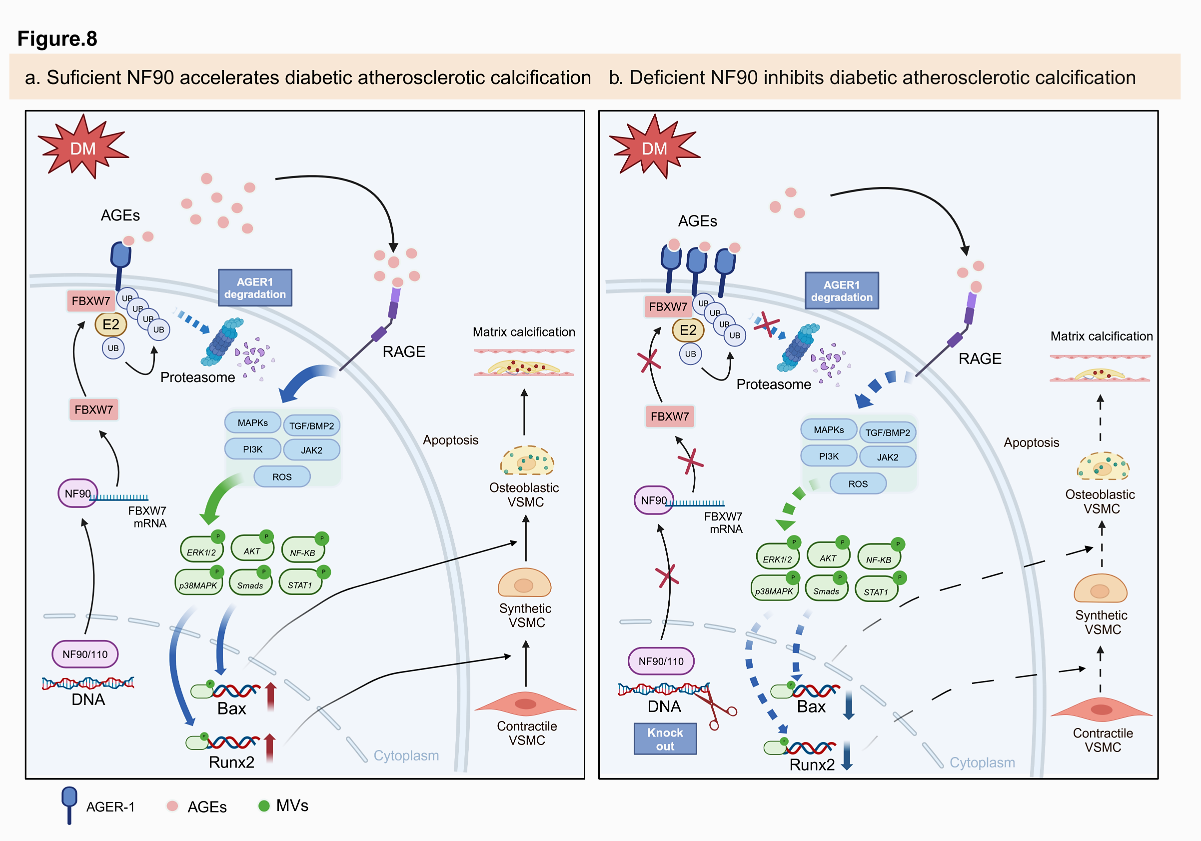
血管钙化是常见的糖尿病血管并发症,是导致糖尿病患者死亡、卒中和下肢截肢的重要因素,但血管钙化的机制不明,缺乏有效的干预靶点和治疗方法。以往研究提示,持续的高血糖可导致体内糖基化终末产物(AGEs)增加,后者通过AGEs受体促进血管钙化的发生和发展。然而,糖尿病导致AGEs积累的机制未明。白细胞介素增强子结合因子 3(ILF3)是一种双链 RNA 结合蛋白,包括NF90和NF110两种亚型,参与调节 DNA 的转录、翻译、mRNA 的稳定性和非编码 RNA 的生物合成。大型队列研究发现,ILF3 和心血管疾病相关,但 ILF3 和糖尿病血管钙化之间的关系不明。
在张运院士指导下,齐鲁医院心内科和急诊科研究团队密切合作,发现在糖尿病患者和糖尿病血管钙化小鼠模型中,平滑肌细胞(VSMC)中的ILF3的NF90亚型表达上调,平滑肌细胞中AGEs水平上升,增多的AGEs作用于特异性受体RAGE,激活多条下游信号通路,促进VSMC 的表型转化和凋亡以及基质囊泡的释放,最终加速糖尿病血管钙化的发生与发展。深入研究发现,NF90的激活可通过增强泛素化蛋白酶FBXW7 mRNA的稳定性并上调其表达,引发AGEs的清除受体AGER1 (负责清除体内AGEs的主要受体蛋白)的泛素化和蛋白酶体降解,导致AGEs细胞内的清除受阻和快速积累,最终加速糖尿病血管钙化的发生。相反,VSMC特异性敲除NF90后,FBXW7表达下调,AGER1蛋白水平升高,AGEs在细胞内的积累减少,糖尿病血管钙化受到显著抑制。随后,课题组利用敲除FBXW7的补救实验证实了NF90通过FBXW7-AGER1-AGEs通路介导糖尿病血管钙化的分子机制,为糖尿病血管钙化提供了新的干预靶点。该研究近日发表于Nature Communications,齐鲁医院心血管实验室张铭湘教授、急诊科陈玉国教授和心内科张运院士为该文的共同通讯作者,齐鲁医院急诊科博士后谢飞博士、刘斌博士和心内科乔温博士为该文的共同第一作者,山东大学齐鲁医院为该文的第一和通讯作者单位。
腹主动脉瘤(Abdominal aortic aneurysm, AAA)是一种严重的大血管疾病,一旦破裂,死亡率超过80%。AAA的病理特征是主动脉的不可逆性扩张,伴有管壁炎症、蛋白水解活性增强和细胞外基质降解。近年研究表明,促炎和抗炎反应之间的不平衡在AAA的发展中起着关键作用。然而,AAA的发病机制不明,治疗药物欠缺。
白细胞介素增强结合因子3(ILF 3)作为一种双链RNA结合蛋白,是已知的先天性免疫反应的调节剂,与心血管疾病密切相关,但ILF 3在AAA中的作用和机制不明。齐鲁医院心内科张铭湘教授课题组研究发现,在AAA患者和血管紧张素II (Ang II)诱导的AAA小鼠模型中,ILF3表达水平明显升高,且主要在巨噬细胞中表达。因此,该课题组构建了巨噬细胞特异性ILF3过表达小鼠(ILF3M-Tg)和巨噬细胞特异性ILF3敲除小鼠(ILF3M-KO),在Ang II和CaCl2诱导的AAA小鼠模型中,发现巨噬细胞ILF3敲除显著减轻了AAA进展,而巨噬细胞ILF3过表达则加重AAA进展。为进一步阐明巨噬细胞ILF3在AAA发病中的作用和机制,课题组通过scRNA-seq,发现巨噬细胞ILF3与免疫应答相关的信号通路显著相关。 深入研究发现,巨噬细胞ILF3通过调控NF-κB和Keap 1-Nrf 2途径,导致巨噬细胞中促炎与抗炎反应的失衡,进而介导了AAA的发生。
目前,AAA的治疗主要以外科手术为主,缺乏针对性药物,单纯的抗炎药物疗效不佳。甲基巴多索隆(BM)已被证明是Keap 1-Nrf 2通路的激活剂和NF-κB途径的抑制剂。课题组利用BM治疗AAA,发现BM可逆转巨噬细胞ILF3过表达所引起的血管扩张,有望成为治疗AAA的有效药物。总之,该研究发现了巨噬细胞ILF3在AAA中的重要作用和机制,为AAA的干预提供了新靶点和新药物。该研究近日发表于Nature子刊Nature Communications,齐鲁医院心血管实验室张铭湘教授、急诊科陈玉国教授、心内科张运院士和首都医科大学安贞医院心内科姜文剑教授为该文的共同通讯作者,齐鲁医院心内科博士生王朝阳(现为山东省立医院心内科医师)和程杰为该文的共同第一作者,山东大学齐鲁医院为该文的第一和通讯作者单位。

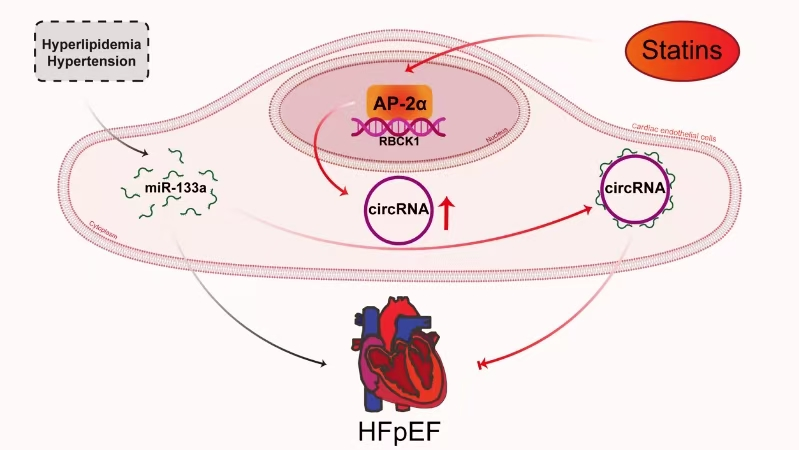
射血分数保留性心力衰竭(HFpEF)是心力衰竭的一种亚型,其特征是左室射血分数正常,但左室舒张功能受损,导致心脏在舒张期充盈受损和收缩期射血减少。随着全球老龄化趋势的加剧,HFpEF的发病率逐年上升,但临床治疗手段受限。血管内皮功能异常是众多心血管疾病的始动因素,心脏中内皮细胞数目约占总细胞数目的45%,因此靶向心脏内皮细胞有可能成为治疗HFpEF的潜在途径。本课题组前期研究发现,他汀类药物可通过miR-133a/GTPCH1途径改善多种环境危险因素所引起的血管内皮功能异常(Circulation,2016, 29;134(22):1752-1765),但他汀对HFpEF的作用不明。齐鲁医院王双喜教授领导的课题组采用生物信息学、分子生物学、细胞生物学和模式动物学等多项实验手段,发现洛伐他汀在心脏血管内皮细胞(主要是心内膜内皮细胞和冠脉微循环内皮细胞)通过激活转录因子AP-2α上调circRNA-RBCK1的表达。深入研究发现,circRNA-RBCK1通过海绵吸附效应抑制miR-133a的功能,从而增加GTPCH1基因的表达。在代谢异常和血流动力学异常双重因素所诱发的HFpEF小鼠模型中,洛伐他汀改善了左室的舒张功能,该效应可被内皮特异性敲除AP-2α或沉默circRNA-RBCK1所阻断。总之,该研究揭示了他汀类药物可通过靶向心脏内皮细胞AP-2α/circRNA-RBCK1/miR-133a/GTPCH1途径改善左室的内皮依赖性舒张功能,为HFpEF的防治研究提供了新思路。该研究近日发表于Nature子刊Nature Communications,齐鲁医院心血管实验室王双喜教授、新乡医学院李鹏教授和山东省立医院心内科董波教授为该文的共同通讯作者,齐鲁医院心血管实验室李彬博士、中医科白文武副教授和心内科郭涛副教授为该文的共同第一作者,山东大学齐鲁医院为该文的第一和通讯作者单位。