[本站讯]近日,山东大学基础医学院马春红教授和武专昌副教授为共同通讯作者在Nucleic Acids Research(5年IF=16.8)上发表题为“hnRNPA2B1 induces HBV cccDNA degradation by recruiting APOBEC3B”的研究成果,揭示了宿主通过hnRNPA2B1招募APOBEC3B诱导cccDNA胞嘧啶脱氨基编辑与降解,限制HBV复制的新机制。基础医学院博士研究生傅振东为该论文的第一作者,山东大学为该论文的第一作者单位和通讯作者单位。
HBV慢性感染是肝癌发生的重要诱因和全球备受关注的重大公共卫生问题。HBV特殊复制模板-共价闭合环状 DNA(cccDNA)结构稳定,半衰期长,不易被降解,是慢乙肝难以治愈的重要原因。而现有临床药物并不能靶向cccDNA,亟需揭示cccDNA稳定性调控机制,发现干预新靶点。
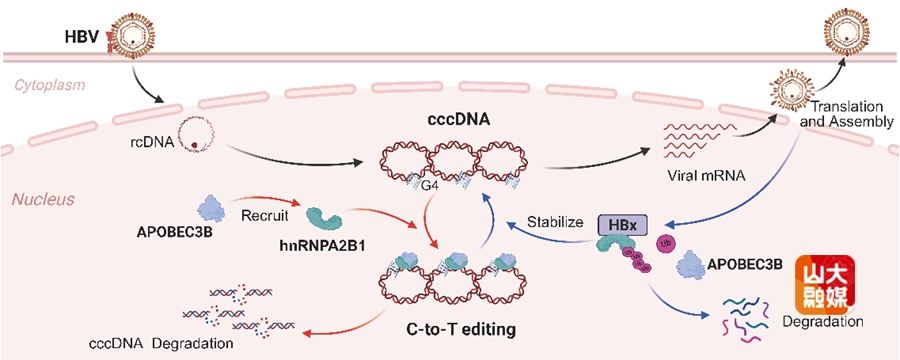
本研究通过cccDNA-宿主互作筛选,鉴定出异质核核糖核蛋白A2/B1(hnRNPA2B1)为一种新型HBV宿主限制因子,其可结合并促进cccDNA降解。机制上,hnRNPA2B1识别cccDNA上的G-四链体(G4)结构(尤其偏好G4-1、G4-7和G4-10位点),并通过其PrLD结构域招募胞苷脱氨酶APOBEC3B,进而引发cccDNA C>T高频编辑,导致A/P位点产生与降解。而HBV通过其HBx蛋白介导hnRNPA2B1的多聚泛素化及蛋白酶体降解,削弱这一宿主防御机制,维持cccDNA的稳定性。该研究揭示了HBV拮抗宿主hnRNPA2B-APOBEC3B降解通路,维持cccDNA稳定存在的新机制,不仅深化了对cccDNA持续存留的认识,也为HBV抗病毒治疗提供了潜在新靶点。
马春红教授团队长期致力于免疫与HBV相关肝病研究,系统探索HBV、代谢等环境因素诱发肝脏炎症及其恶性转化机制,近年围绕HBV与宿主互作,发现了调控cccDNA稳定性和转录活性的多个宿主因子-hnRNPA2B1、ABCF1、Cohesin和linc01431,相关研究成果发表在Nucleic Acids Res、Cell Mol Gastroenterol Hepatol、Cell Mol Immunol、Adv Sci等国际知名期刊。该工作得到了国家重点研发计划、国家自然科学基金创新群体项目、山东省自然科学基金优青项目、泰山学者等项目资助。