[本站讯]近日,齐鲁医院神经外科李刚/薛皓教授团队在胶质母细胞瘤化疗耐药机制及临床“老药新用”研究领域取得新进展。研究团队创新性地揭示了临床一线抗癫痫药物—左乙拉西坦(Levetiracetam, LEV)能够通过阻断肿瘤细胞囊泡外排途径,逆转胶质母细胞瘤对替莫唑胺(Temozolomide, TMZ)的化疗耐药新机制,从而显著提升了化疗敏感性。相关研究成果以“Levetiracetam Reverses Temozolomide Resistance in Glioblastoma by Blocking Drug Efflux through RAB5A/CD63-RAB35 Axis”发表于国际肿瘤学期刊Cancer Letters(中科院1区,IF:10.1)。神经外科教授李刚、薛皓,副教授张开亮为共同通讯作者。神经外科博士后赵吉星、硕士研究生李明坤为共同第一作者。齐鲁医院为第一作者和通讯作者单位。

脑胶质瘤患者在术后及疾病进展过程中常伴发癫痫,抗癫痫药物的应用是临床必不可少的环节;然而,脑胶质瘤患者的抗癫痫药物的选择策略尚缺乏精准和个性化指导。团队针对该临床问题,通过前期的临床队列研究,发现使用抗癫痫药物的脑胶质瘤患者中仅左乙拉西坦表现出了显著的生存获益,进一步通过大规模临床队列研究和一系列深入的基础实验研究,最终确认左乙拉西坦具备显著的抗肿瘤协同作用。这一发现首次拓展了抗癫痫药物的抗肿瘤临床应用场景,为脑胶质瘤患者的抗癫痫用药选择提供了循证依据。
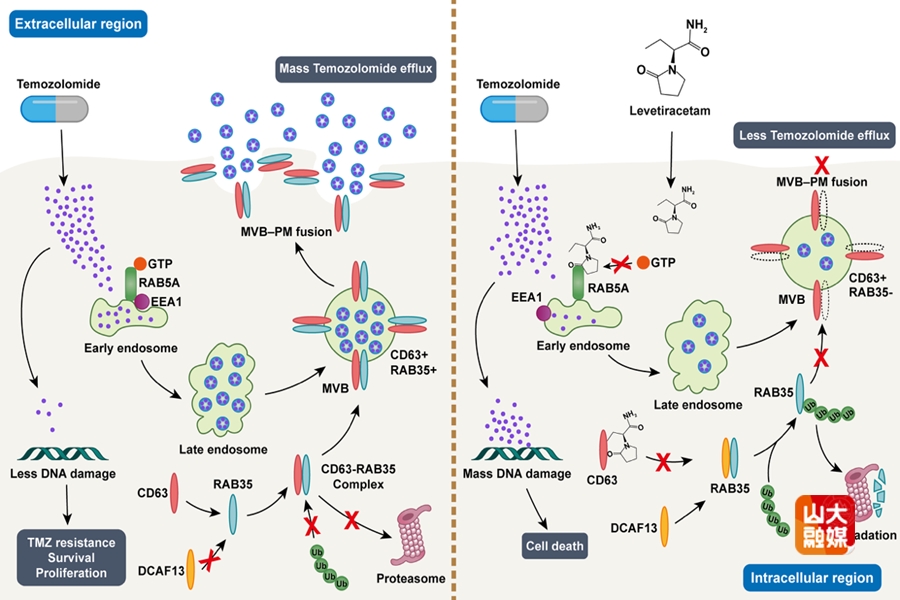
本次发表的成果是该团队在左乙拉西坦抗肿瘤分子机制探索上取得的又一项重要进展。本研究揭示了一条非癫痫药理靶点、非神经元依赖的全新抗肿瘤机制,即左乙拉西坦作为细胞外囊泡分泌抑制剂,靶向阻断肿瘤细胞囊泡外排清除化疗药物,进一步丰富了左乙拉西坦在胶质瘤综合治疗中的理论基础。团队利用化学蛋白质组学技术深入研究,揭示了胶质母细胞瘤通过“囊泡外排”清除化疗药物的耐药新机制。肿瘤细胞可通过“内体–多囊泡体–外泌体”这一囊泡运输途径,将进入细胞内的化疗药物替莫唑胺向胞外排出,从而降低细胞内有效药物浓度,导致化疗耐受。本研究证实,左乙拉西坦能够精准靶向RAB5A/CD63-RAB35囊泡转运轴,一方面竞争性结合RAB5A,阻断替莫唑胺的内体转运;另一方面破坏CD63-RAB35复合体,促进RAB35降解并抑制外泌体释放。研究表明,左乙拉西坦能够有效阻断肿瘤细胞向外排泌化疗药物的通道,使更多的替莫唑胺滞留在肿瘤细胞内,从而增强对肿瘤细胞的杀伤效应。
该发现突破了长期以来替莫唑胺耐药研究主要聚焦于DNA损伤修复(如MGMT表达)的传统框架,证实了“囊泡介导的药物外排”是肿瘤产生化疗耐受的重要非经典机制。此外,团队还构建了基于囊泡外排分子标志物CD63/RAB35表达的替莫唑胺耐药评分体系,为筛选左乙拉西坦潜在获益人群提供了可靠的诊断依据和标准,具有重要的临床转化价值。团队提出的“抗癫痫药物(左乙拉西坦)+一线化疗药物(替莫唑胺)”联合治疗策略,为克服脑胶质瘤化疗耐药提供了新的干预方案,也为脑胶质瘤患者术后抗癫痫药物的优选策略提供了坚实的科学依据。
李刚/薛皓教授团队长期致力于脑胶质瘤发生发展机制、分子标志物鉴定及精准诊疗新策略研究,围绕胶质瘤细胞外囊泡、肿瘤微环境、神经–肿瘤互作及治疗抵抗等方向持续开展系统性工作,取得了一系列研究成果。该研究得到了国家自然科学基金、山东省重点研发计划、泰山学者攀登计划、青年泰山学者计划等项目资助,同时得到山东省脑健康与功能重构重点实验室、山东大学脑与类脑科学研究院等平台支持。